動画版はこちら↓
アスピリンとは?
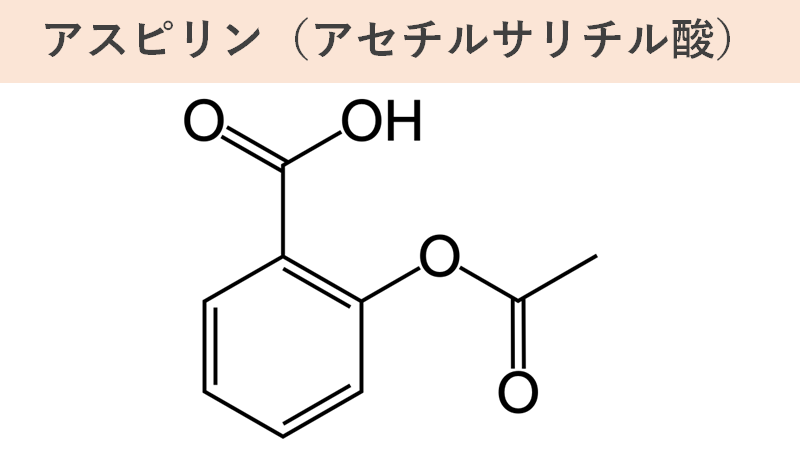
アスピリンはドイツのバイエル社から発売された「アセチルサリチル酸製剤」の商標名です。アスピリンは人類史上最も使用された医薬品かつ人類で初めて合成された医薬品です。開発から110年以上経過したにも関わらず、現在でも広く使用されている薬はおそらく他にはないでしょう。
アスピリンの名前の由来は、アセチルサリチル酸の頭文字である「A」と、サリチル酸のドイツ名である「spir saure(スピール酸)」を組み合わせて命名されました。更に、その「spir saure」はセイヨウナツユキソウのラテン異名であるSpiraea ulmariaの属名である「Spiraea」に由来しています。したがって、名前的によく「ピリン系」の薬剤と勘違いされますが、実はそうではありません。
アスピリンの誕生
古くから、「葉の裏が白いヤナギの樹皮には解熱・鎮痛作用がある」ということが知られており、2500年ほど前にヒポクラテスによって発熱・痛みの治療薬として用いられていたようです。他にも、分娩時の痛みを和らげるため、通風や神経痛に対する鎮痛を目的に広く用いられていた記録が存在しています。日本でもその鎮痛作用は知られていたようで、歯痛に効果があるとしてヤナギを爪楊枝にして用いていました。しかし、どのような物質がどうやって痛みを抑えていたのかは長い間不明なままでした。
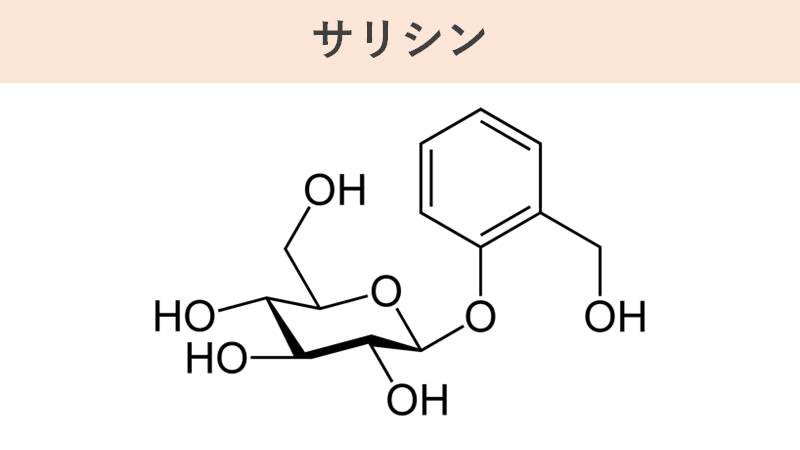
1763年、イギリスの神父であったストーンがヤナギの樹皮から抽出したエキスに解熱・鎮痛作用があることを発見します。彼はその物質をヤナギの学名にちなんで「サリシン」と名付けました。これは相当に苦味が強かったらしく、解熱鎮痛作用があるとはいえ服用はかなりきつかったようです。しかし、西洋人にはきつく感じたようですが、漢方薬を服用していたアジア人にとってはそこまででもなかったという話もあります。
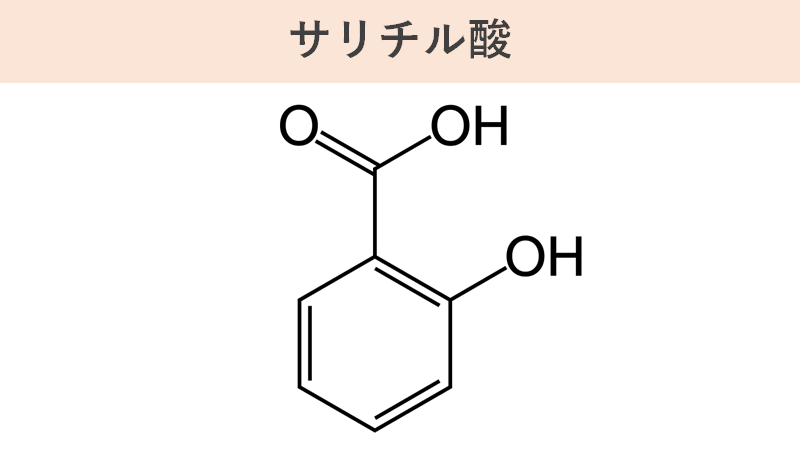
それからしばらく後の1838年、フランスの薬剤師であるルルーとイタリアの科学者であるピリアによって、サリシンを分解すると「サリチル酸」が得られるということが発見されました。そして、そのサリチル酸が鎮痛剤として使えることも判明しました。サリチル酸は解熱鎮痛剤として用いられましたが、胃粘膜を直接刺激するために強い胃腸障害作用を持っていて、吐き気や胃潰瘍などの副作用が発現するや苦みが強いなどの問題を抱えていました。したがって、その扱いにくさを改善した薬の出現が待ち望まれていました。
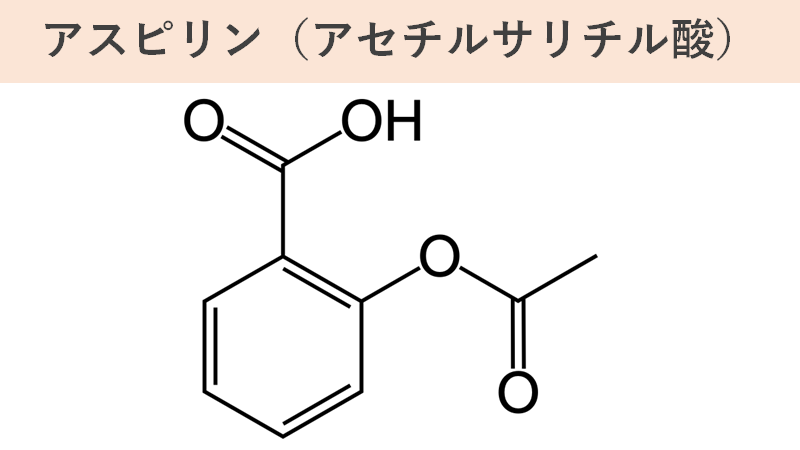
そんなサリチル酸の改良に、バイエル社で研究を行っていたフェリックス・ホフマンも着手していました。彼の父は関節リウマチを患っており、サリチル酸の副作用に悩む父のためより良い薬を作りたいと考えていました。その研究が実を結んだのが1897年、サリチル酸をアセチル化した「アセチルサリチル酸」が合成されました。アセチルサリチル酸はサリチル酸より副作用が少ないということが分かっています。
今紹介したフェリックス・ホフマンの話は有名ですが。真の功労者はユダヤ人であったアルトゥル・アイヒェングリュンだったという話もあるようです。このことはナチスの政策の関係で隠蔽されたとかなんとか…。
アセチルサリチル酸は、1899年にバイエル社によって「アスピリン」の商標で登録されました。その後、1900年には早くも錠剤として発売され、20世紀の初頭にはバイエル社の売り上げの3割程度を占めるほど売れました。世間がどれほど有用な痛み止めを待ち望んでいたかわかるような気がします。
商標登録とアスピリン
アスピリンはドイツのバイエル社によって商標登録がされていました。しかし、第一次世界大戦後、商標が連合国側に取り上げられ、アメリカのスターリング・プロダクツ社に売却されました。しかし、スターリング社は商品名を「バイエルアスピリン」と変えずにそのまま販売しています。これにはアスピリンの特許が切れた後の後発医薬品が軒並み微妙だったため、信頼と安心の「バイエルアスピリン」という感じだったのでしょう。そのような流れがあり、アスピリンは一般名となってしまいます。日本では1932年以来日本薬局方に一般名の「アスピリン」で収載されました。
アスピリン作用機序と新たな用途
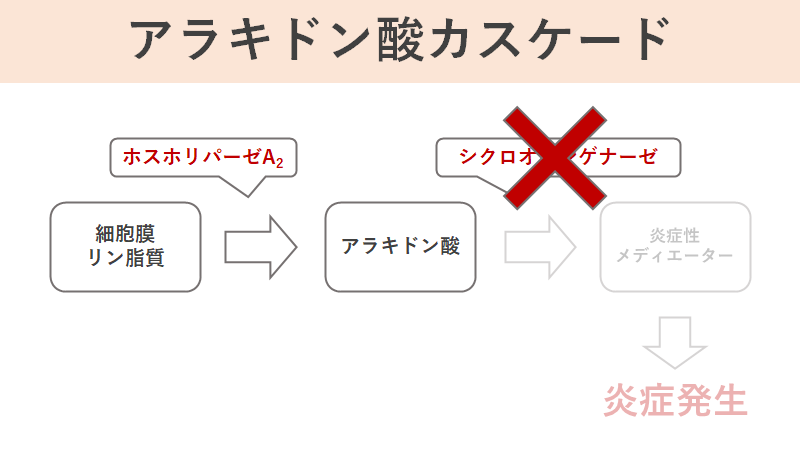
アスピリンは1899年から販売されている医薬品ですが、炎症を抑える機序が明らかになったのはなんとそれから約70年後の1971年です。アスピリンの鎮痛作用は「炎症性メディエーターの合成阻害」によって得られているということが示されました。機序の詳細は別記事で解説しているのでここでは省略します。
一方、アスピリンが大量に使用されるようになって、とある現象が発生するようになっていきました。それは、アスピリンを痛み止めとして使用すると手術後の出血が多くなる、心筋梗塞にかかる人の数が減少したといった変化でした。そのため、1950年代になるとアスピリンには別の機能もあるのではないか?と指摘されるようになっていました。その後、研究が重ねられ、低用量のアスピリンには脳梗塞や狭心症の予防効果があるということが示されました。そのため、アスピリンは脳梗塞などの疾患を予防するためにも用いられるようになりました。そして、実はこの血小板の機能を抑制する作用はアスピリンにのみ認められている作用で、他のサリチル酸誘導体では見られません。
ただし、皮下出血や鼻血などの出血が発生する頻度も高くなることも判明しました。
アスピリンの体内動態
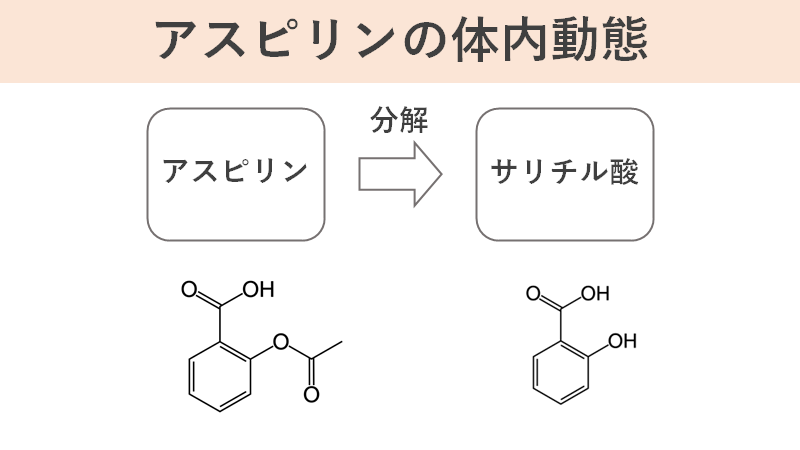
アスピリンは消化管から吸収後、腸管や肝臓、血中で速やかに加水分解を受けてサリチル酸になります。そのためアスピリンの半減期は短く、常用量では15分程度です。サリチル酸はそれから全身循環に移行し、効果を発揮していきます。
アスピリンの毒性
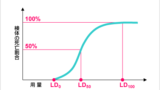
それではここからアスピリンの毒性についてみていきます。最初はLD50(Lethal Dose 50:半数致死量)についてみていきます。LD50については別記事を参考にして下さい。

ヒトの摂取量では150mg/kg・体重までは無症状、500mg/kg・体重を超えると致死的になると言われています。添付文書上では最大量が1日4.5gまでなので、相当量摂取しない限り急性中毒は問題ないと思われます。

主な症状としては、過換気、耳鳴、嘔吐等が挙げられます。他には、高体温もよく見られるようです。錯乱、傾眠、けいれんなども生じる可能性があります。致死的になりやすいのが代謝性アシドーシスによって心機能が障害され、心不全、不整脈が発生することであると言われています。
アスピリンの毒性機序
アスピリンの作用機序は、
サリチル酸が酸化的リン酸化を脱共役することで好気性代謝を阻害し、嫌気性代謝が亢進する
となります。
今回の機序ではアスピリンが問題を起こすというよりは、分解して発生するサリチル酸が問題になってきます。サリチル酸は比較的簡単に細胞膜を通過する性質を持っているため、体内で発生したサリチル酸は全身の細胞に続々侵入していき問題を引き起こします。
電子伝達系とは?
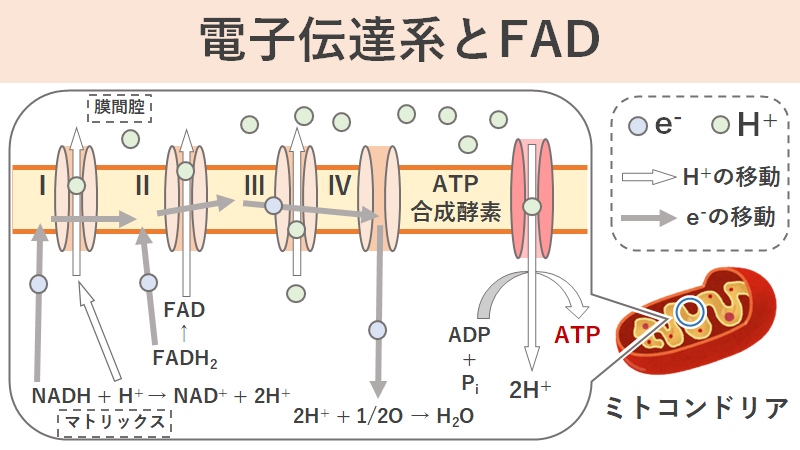
電子伝達系とはミトコンドリア内で行われるATPを合成する一連の反応系のことです。そこで作られるATPは細胞の生命維持や細胞の活動に必要になるため非常に重要な物質です。
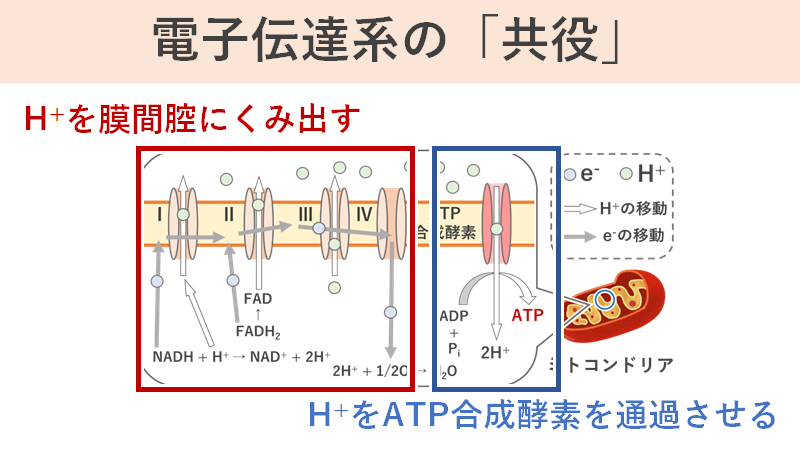
電子伝達系の具体的なメカニズムについては省略しますが、ミトコンドリアの内膜と外膜に発生したH+濃度の差を利用してH+の流れを生み出し、その流れをATP合成酵素に通すことでATPを合成しています。つまり、「H+の濃度勾配を生み出す反応」と「H+がATP合成酵素を通過してATPが合成される反応」がセットになって機能しています。この事を「共役」といいます。
脱共役剤「サリチル酸」
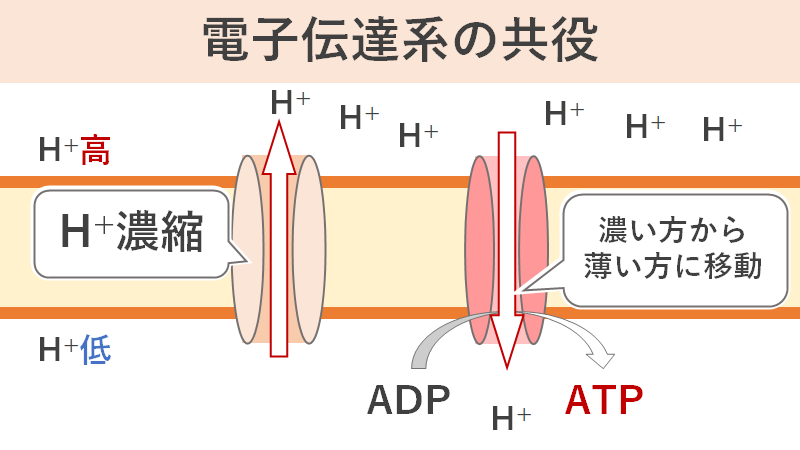
「脱共役」とは、共役して働いているそれぞれの反応系は阻害せずに、それぞれの連携を阻害する事を言います。上図は電子伝達系で行われている共役を簡単に図にしたものです。左側の複合体たちで膜間腔へH+を濃縮し、濃縮されたH+はATP合成酵素を通ってマトリックスへ戻っていきます。この時にATP合成酵素がATPを合成してます。そこにサリチル酸が大量に侵入するとここに変化が生じます。
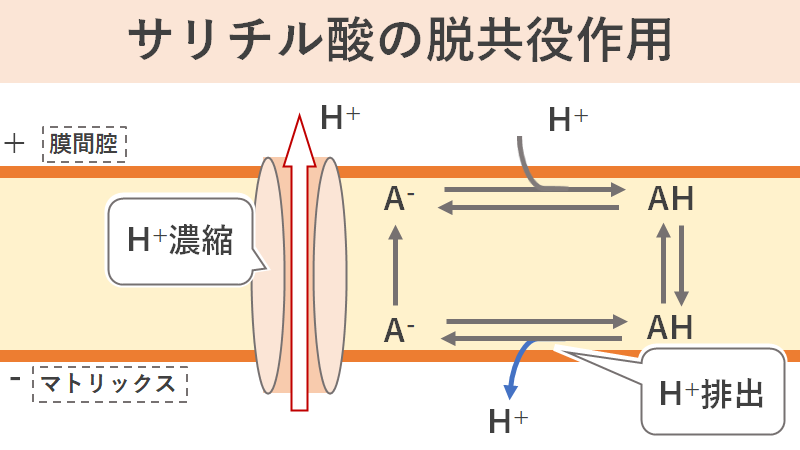
サリチル酸は弱くはありますが、脱共役作用を持っています。先ほどATPの合成にはH+の濃度勾配を作ることが不可欠と解説したと思いますが、サリチル酸はミトコンドリアに作用し、勝手にH+を外に汲み出す作用を持っています。そのため、ミトコンドリアが必死に作ったH+の濃度変化を勝手に消滅させてしまうのです。その結果、ミトコンドリア内のH+濃度勾配がなくなってしまうため、ATPの合成ができなくなってしまいます。ATPは細胞の活動に欠かせないエネルギーなので、細胞の生命活動が障害されてしまいます。
好気性代謝から嫌気性代謝へのシフト
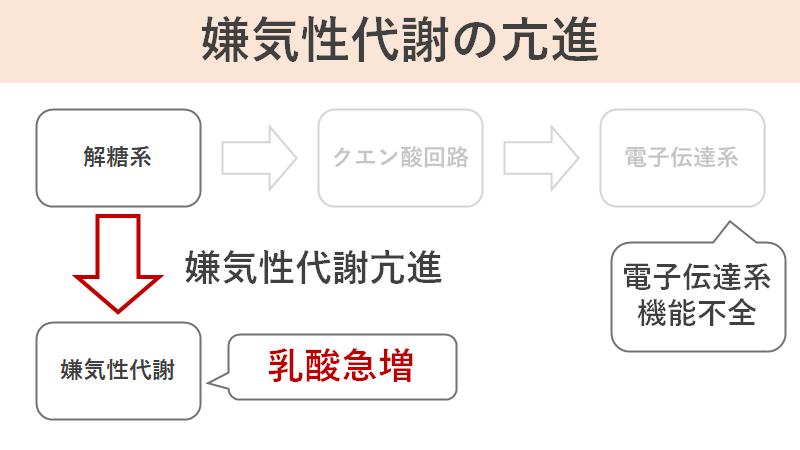
好気性代謝が阻害されたとしても、細胞にはまだエネルギーを作る方法が存在しており、それが「嫌気的代謝」です。嫌気性代謝が亢進すると乳酸の産生が亢進されることとなります。また、他のエネルギー産生経路も活用され、脂質の代謝も活発になります。その結果、アセト酢酸やβ‐ヒドロキシ酪酸等といった物質が発生します。
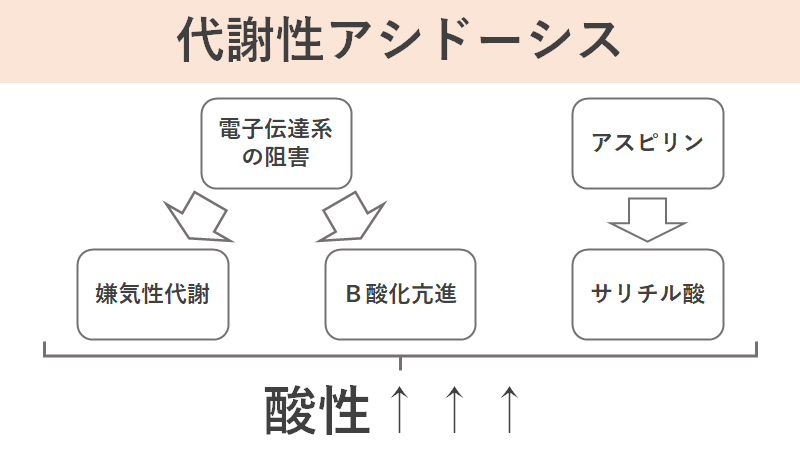
嫌気性代謝の亢進によって乳酸をはじめとした酸性の物質が急激に増えること、かつアスピリンやそれが分解されて発生し得たサリチル酸が血中にどんどん増加し、血液が酸性に傾いて行きます。これを代謝性アシドーシスといいます。

代謝性アシドーシスによって生じる症状はかなり多くあるため、今回はその一例を示しました。これらの症状が同時に発生し、様々な方向から生命維持を困難にしていきます。このため、




コメント